גרפיט, נוסחה מולקולרית: C, משקל מולקולרי: 12.01, הוא צורה של יסוד פחמן, כל אטום פחמן מחובר על ידי שלושה אטומי פחמן אחרים (המסודרים במשושים של חלת דבש) ליצירת מולקולה קוולנטית. מכיוון שכל אטום פחמן פולט אלקטרון, אלו שיכולים לנוע בחופשיות, לכן גרפיט הוא מוליך.
גרפיט הוא אחד המינרלים הרכים ביותר, והשימושים בו כוללים ייצור מובילי עיפרון וחומרי סיכה. פחמן הוא יסוד לא מתכתי הממוקם בקבוצת המחזור השני IVA של הטבלה המחזורית. גרפיט נוצר בטמפרטורות גבוהות.
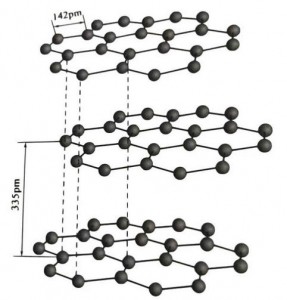
הגרפיט הוא מינרל גבישי של יסודות פחמן, והסריג הגבישי שלו הוא מבנה שכבות משושה. המרחק בין כל שכבת רשת הוא 3.35A, והמרווח של אטומי פחמן באותה שכבת רשת הוא 1.42A. זוהי מערכת קריסטל משושה עם מחשוף שכבות שלם. משטח המחשוף הוא בעיקר קשרים מולקולריים, פחות אטרקטיביים למולקולות, ולכן הציפה הטבעית שלו טובה מאוד.
בגבישי גרפיט, אטומי הפחמן באותה שכבה יוצרים קשר קוולנטי עם הכלאה של sp2, וכל אטום פחמן מחובר לשלושה אטומים אחרים בשלושה קשרים קוולנטיים. ששת אטומי הפחמן יוצרים טבעת רציפה של שש באותו מישור, המשתרעת לתוך מבנה למלה, כאשר אורך הקשר של קשר ה-CC הוא 142pm, שזה בדיוק בטווח אורך הקשר של הגביש האטומי, כך של אותה שכבה. , זהו גביש אטומי. לאטומי פחמן באותו מישור יש מסלול p אחד, שחופפים זה את זה. האלקטרונים חופשיים יחסית, שוות ערך לאלקטרונים חופשיים במתכות, ולכן גרפיט יכול להוליך חום וחשמל, המאפיין את גבישי המתכת. כך גם מסווג כגבישים מתכתיים.
השכבה האמצעית של גביש גרפיט מופרדת על ידי 335pm, והמרחק גדול. הוא משולב עם כוח ואן דר ואלס, כלומר, השכבה שייכת לגביש המולקולרי. עם זאת, מכיוון שהקישור של אטומי פחמן באותה שכבת מישור חזקה מאוד וקשה ביותר להרוס, גם נקודת הפירוק של הגרפיט גבוהה מאוד והתכונות הכימיות שלו יציבות.
לאור מצב ההדבקה המיוחד שלו, לא ניתן להתייחס אליו כגביש יחיד או כפולי גביש, גרפיט נחשב כיום כגביש מעורב.
זמן פרסום: 31 ביולי 2023